
- 텍스트 축소
- 확대
美 휴미라 바이오시밀러 '바이오금맥' 부상…올해부터 '처방 경쟁'
- 송고 2023.06.27 04:00 | 수정 2023.06.27 04:00
- EBN 김남희 기자 (nina@ebn.co.kr)
에피스, 2018년 4분기~올 1분기 누적매출 1조2100억원
유럽·미국·캐나다 이어 한국에서 고농도 제형 허가 획득
삼성에피스·셀트리온 고농도 '휴미라' 바이오시밀러 허가

삼성바이오에피스가 고농도 휴미라(성분명 아달리무맙) 바이오시밀러 국내 품목허가를 획득하면서, 국내에서 고농도 제형을 출시한 셀트리온과의 경쟁 구도에 시선이 모아진다.ⓒ삼성바이오에피스
삼성바이오에피스가 고농도 휴미라(성분명 아달리무맙) 바이오시밀러 국내 품목허가를 획득하면서, 국내에서 고농도 제형을 출시한 셀트리온과의 경쟁 구도에 시선이 모아진다.
27일 바이오시밀러 업계에 따르면 올해부터 미국 휴미라 바이오시밀러 시장 경쟁이 개막됐다. 글로벌 시장에서 단지 5%만 차지해도 1조원에 육박하는 매출을 달성할 정도로 세계 시장에서 치열한 휴미라 바이오시밀러 시장은 막강한 영향력을 갖고 있다.
미국 애브비사가 개발한 블록버스터 의약품 휴미라의 연 매출은 212억달러(한화 약 28조원‧2022년 기준)로 조사됐다. 휴미라의 물질특허 만료(유럽 2018년‧미국 2016년) 시점에 맞춰 전 세계적으로 바이오시밀러 개발 경쟁이 돌입됐다. 국내 기업으로는 삼성바이오에피스(이하 삼성에피스)와 셀트리온이 양대 플레이어가 되어 활약하고 있다.
삼성에피스는 2017년 8월 유럽에서, 2019년 7월 미국에서 휴미라 바이오시밀러의 판매 허가를 획득했으며 2018년 10월부터 유럽 시장에서 제품을 판매하고 있다. 유럽 제품명은 임랄디로 바이오젠이 판매 중이다.

ⓒ삼성바이오에피스
유럽 시장에서는 2018년 10월에 먼저 휴미라 바이오시밀러 시장이 개막됐다. 현재까지 유럽에서 출시된 휴미라 바이오시밀러 제품은 총 7종이며, 판매량 기준 휴미라의 유럽 내 시장 점유율은 현재 40% 미만으로 하락한 것으로 집계됐다.
올해 7월부터는 미국 시장에서도 휴미라 바이오시밀러가 출시될 예정이다. 앞서 휴미라는 지난해 미국에서만 매출 186억달러(한화 약 24조원)를 기록했다. 현재 미국 시장에서 품목 허가를 획득한 휴미라 바이오시밀러는 총 9종에 달한다.
고농도 제형으로 전선(戰線) 확대…포트폴리오 다각화
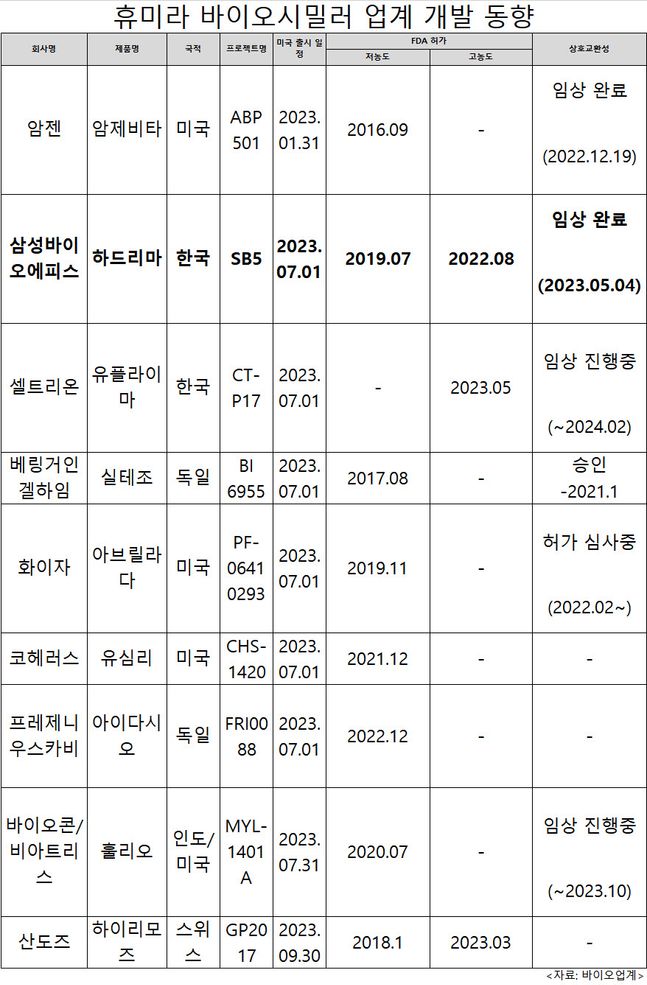
시장 경쟁이 치열하다보니 고농도 제형으로 경쟁력을 키워 전선을 확대하는 움직임도 포착되고 있다. 글로벌 제약사인 애브비는 오리지네이터의 경쟁력 강화를 위해 기존 제형에서 용법용량 등을 개선한 고농도 제형의 휴미라를 개발해 2015년에 FDA 허가를 받은 바 있다. 이후 고농도 중심으로 시장을 전환해 현재 휴미라는 미국 시장에서 약 80% 이상의 비중으로 고농도 제형이 처방되고 있다는 게 업계의 설명이다.
ⓒ
이같은 시장 상황에 발맞춰 바이오시밀러 기업들도 고농도 제형 확보에 적극 나서고 있다. 에피스는 지난해 8월 미국에서 최초로 고농도 휴미라 바이오시밀러 제형의 허가를 받아 업계에서 유일하게 저농도와 고농도 바이오시밀러 포트폴리오를 확보한 기업이 됐다.
에피스 외에도 앞서 저농도 제형으로 판매허가를 받은 암젠, 산도즈 등 글로벌 기업들도 고농도 개발에 추가로 뛰어든 현재 상대적으로 개발이 늦었던 셀트리온은 처음부터 고농도 제형만을 개발 올해 FDA 품목허가를 승인받았다.
상호호환성(Interchangeability 승인 추진도 대세
상호호환성(Interchangeability) 승인 추진도 대세로 자리 잡고 있다. 규정상 바이오시밀러는 오리지널 의약품 대비 비교 연구로 얻은 임상의학적 동등성을 기반으로 한 상호호환성을 가지며, 이를 통해 오리지널 의약품을 대체 처방할 수 있는 물질이다.
다만 미국(FDA)에서는 유럽(EMA)과 달리 상호호환 가능한 바이오시밀러로 공인받기 위해서는 별도의 안전성 및 효능을 입증해야 하는 가이드라인을 갖고 있어 추가 환자 임상을 진행하고 허가 승인 절차를 받아야 한다.

상호호환성(Interchangeability) 승인 추진도 대세로 자리 잡고 있다. 규정상 바이오시밀러는 오리지널 의약품 대비 비교 연구로 얻은 임상의학적 동등성을 기반으로 한 상호호환성을 가지며, 이를 통해 오리지널 의약품을 대체 처방할 수 있는 물질이다.ⓒ픽사베이
이같은 규제 때문에 '인터체인저블(상호호환성) 바이오시밀러’로 승인받으면 미국에서 의사의 개입 없이 약국에서 환자에게 대체 의약품을 처방할 수 있어 환자들에게 더 많은 치료의 대안을 제공할 수 있다는 점이 특징이다.
바이오업계 관계자는 "미국에서의 상호호환성(IC) 승인은 많은 시간과 비용을 추가로 들여야 하지만, 치열한 시밀러 경쟁 속에서 우위를 점할 수도 있는 부분이 있기 때문에 현재 다수의 기업들이 IC 승인을 위한 임상 시험에 뛰어들었다"고 설명했다.
현재 미국 휴미라 바이오시밀러 IC 승인을 받은 기업은 독일 베링거인겔하임의 ‘실테조’가 유일하며, 삼성바이오에피스와 암젠은 임상 시험을 완료한 상태다.
에피스, 올해 1분기까지 누적 제품 매출 1조2100억원
에피스는 휴미라 물질특허 만료에 맞춰 적기에 바이오시밀러 제품을 개발해 유럽과 한국 시장에 출시했다. 미국에서는 2019년 7월 판매 허가를 획득했으며 애브비와의 라이선스 합의에 따라 내년에 출시할 예정이다.
또한 에피스는 마케팅 파트너사인 바이오젠을 통해 유럽에서 임랄디를 판매하고 있으며, 누적 매출은 2018년 4분기부터 2023년 1분기까지 9억2930만 달러(한화 약 1조2100억원)을 기록했다.
ⓒ픽사베이
에피스 관계자는 "이는 회사 매출이 아니라 시장에서 구매된 시장 매출이며, 파트너사와의 계약에 따라 시장 매출을 일정 비율로 정산한 후 회사 매출로 인식한다"고 설명했다.
현재 임랄디의 유럽 시장 점유율은 오리지널 의약품을 포함한 아달리무맙 성분 의약품 전체 시장에서 약 14% 수준이다. 현재 판매 중인 바이오시밀러 제품들(유럽 기준 7종) 중 시장 점유율 상위권을 형성하고 있다는 게 업계의 추산이다.
에피스 측은 “유럽 등 글로벌 시장에서 쌓은 공급 및 판매 노하우와 데이터 경쟁력을 바탕으로 파트너사와 긴밀히 협력하여 미국 휴미라 바이오시밀러 시장을 조기 선점할 수 있도록 노력할 계획이다”고 밝혔다.
©(주) EBN 무단전재 및 재배포 금지
관련기사
전체 댓글 0
서울미디어홀딩스
패밀리미디어 실시간 뉴스






![[EBN 칼럼] 위기의 한국 디스플레이, 탈출구는 바로 여기](https://cdnimage.ebn.co.kr/news/202409/news_1726702349_1637247_c.jpeg)

















