2024 | 09 | 29
23.3℃

많이 본 기사
코스피 2,649.78
▼
21.79(-0.82%)
코스닥 774.49
▼
4.69(-0.6%)
USD$ 1,329.7
▲
1.3
EUR€ 1,486.0
▲
7.3
JPY¥ 917.3
▼
-0.7
CNH¥ 189.4
▼
-0.1
BTC 86,287,000
▼
746,000(-0.86%)
ETH 3,511,000
▼
24,000(-0.68%)
XRP 812.5
▲
36.8(4.74%)
BCH 460,500
▼
16,600(-3.48%)
EOS 705.8
▼
10.2(-1.42%)
- 텍스트 축소
- 확대
씨젠 코로나 진단시약 FDA 긴급사용승인
- 송고 2020.04.22 08:43 | 수정 2020.04.22 08:43
- 동지훈 기자 (jeehoon@ebn.co.kr)
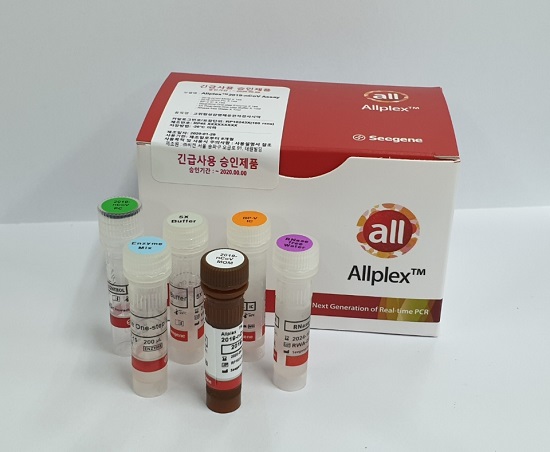
ⓒ씨젠
분자진단 전문기업 씨젠은 미국 식품의약국(FDA)이 자사의 코로나19 검진용 진단시약 '올플렉스(Allplex 2019-nCoV Assay)'의 긴급사용을 승인했다고 22일 밝혔다.
코로나19 검진에 전 세계적으로 사용되고 있는 씨젠의 진단시약은 3개의 목표유전자(E, RdRp, N) 모두를 검출해내는 특징을 갖고 있어 정확도가 높다는 평가를 받는다. 또 한 개의 튜브만으로 검사가 가능해 대량검사를 효율적으로 할 수 있는 장점도 있다.
씨젠은 이번 FDA의 긴급사용승인을 통해 미국의 주요 검진기관들이 코로나19 검사를 위해 자사의 자동 검사 시스템을 통한 대량검사를 진행할 것으로 기대하고 있다.
천종윤 씨젠 대표는 "결과 분석 소프트웨어를 포함한 씨젠의 자동화 시스템은 검사 수행의 편리함과 검사 물량의 확장성으로 인해 지금처럼 수 천건의 검사를 하루 만에 수행해야 하는 감염확산 상황에서 검사량을 대폭 증가시키는데 매우 유용한 것으로 입증됐다"고 말했다.
이어 "기업이 가진 기술을 활용해 필요할 때 사회를 돕는 의무를 충실히 이행하는 한편, 최고의 분자진단기술을 대표하는 우리 진단시약을 미국에 공급하고 있어 자부심을 느낀다"면서 "코로나 바이러스의 수많은 변이까지도 함께 검출할 수 있는 보다 강화된 성능의 제품 개선을 준비하고 있다"고 말했다.
©(주) EBN 무단전재 및 재배포 금지
관련기사
전체 댓글 0
로그인 후 댓글을 작성하실 수 있습니다.
서울미디어홀딩스
패밀리미디어 실시간 뉴스



![[EBN 칼럼] 'Tone at the Top'](https://cdnimage.ebn.co.kr/news/202409/news_1727220614_1637861_c.jpeg)

















